L’alimentation joue un rôle majeur dans la pathogénèse du syndrome de l’intestin irritable. Une activation anormale du système immunitaire, consécutive à l’ingestion d’aliments, serait en jeu, en particulier au niveau de l’intestin grêle.
Plus de 80 % des personnes souffrant du syndrome de l’intestin irritable (SII) rapportent un effet déclenchant ou aggravant de l’alimentation sur leurs symptômes. Si la plupart des études se sont intéressées jusqu’à présent aux anomalies immunitaires au niveau du côlon pour expliquer ces effets de l’alimentation, une revue de littérature examine les mécanismes immunitaires potentiels au niveau de l’intestin grêle.
Les auteurs rappellent tout d’abord le concept de tolérance immunitaire chez les personnes non atteintes de SII (cf. figure 1, partie de gauche). Dans un intestin grêle sain, le système immunitaire tolère la présence d’antigènes alimentaires pour maintenir l’homéostasie. Plus précisément, les antigènes alimentaires sont échantillonnés par les cellules dendritiques puis présentés aux lymphocytes T naïfs, entraînant leur différenciation en lymphocytes T régulateurs puis la libération de cytokines qui suppriment la réponse immunitaire inflammatoire.
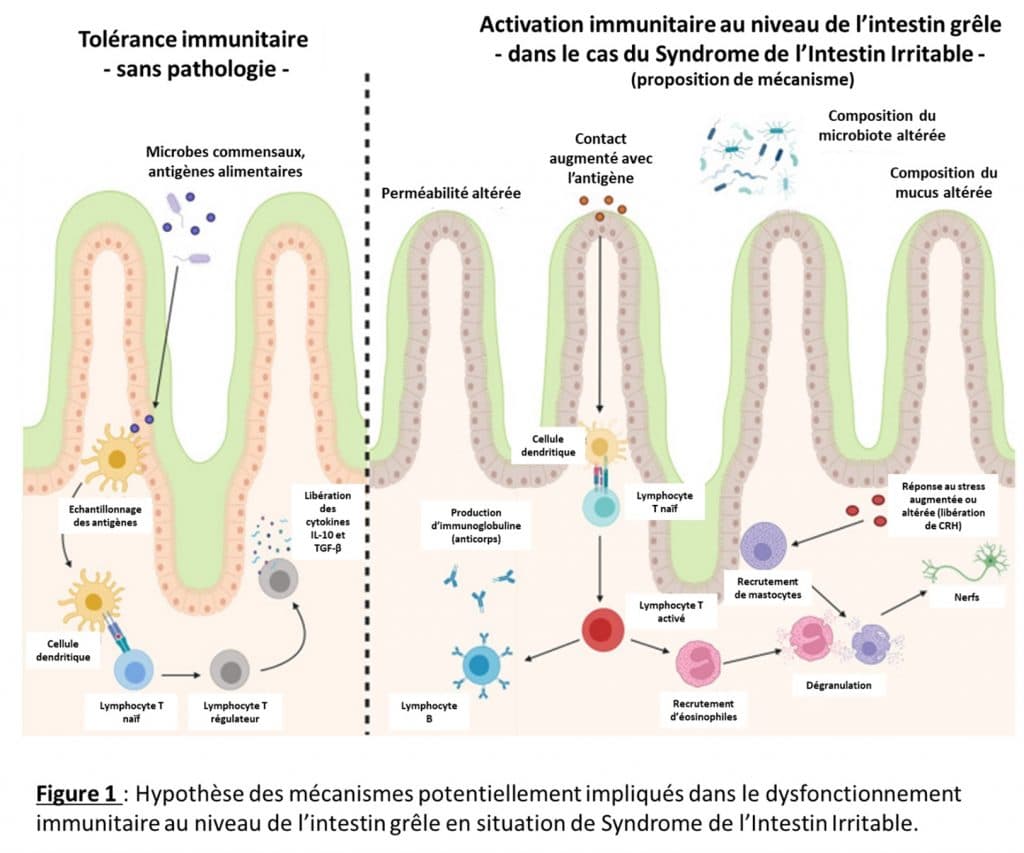
En cas de SII (cf. figure 1, partie de droite), des anomalies physiologiques telles que des altérations de la perméabilité intestinale, de la composition du mucus ou encore de celle du microbiote engendrent un contact augmenté avec les antigènes alimentaires, ainsi qu’une réponse plus forte au stress. Dans ce contexte pathologique, la présentation des antigènes alimentaires pourrait résulter en l’activation des lymphocytes T, la maturation des lymphocytes B et la production d’anticorps spécifiques. Cette activation du système immunitaire ainsi que le stress augmenté provoqueraient par ailleurs le recrutement d’éosinophiles et de mastocytes et la libération de médiateurs inflammatoires qui activeraient le système nerveux entérique entraînant ainsi des douleurs viscérales.
Pour conclure, les auteurs insistent sur l’importance de considérer l’entièreté du tractus gastro-intestinal et non plus uniquement le côlon, dans l’objectif de mieux comprendre les mécanismes immunitaires liés au SII.
BURNS, GL. TALLEY, NJ. & KEELY, S. Immune responses in the irritable bowel syndromes: time to consider the small intestine. BMC Medicine, 2022, 20, 115, doi: 10.1186/s12916-022-02301-8.
